Các công ty cho biết vaccine đã tạo ra phản ứng miễn dịch ở trẻ từ 5 đến 11 tuổi trong thử nghiệm lâm sàng Giai đoạn II / III, phù hợp với những gì họ đã quan sát trước đó ở những người từ 16 đến 25 tuổi. Họ nói rằng hồ sơ an toàn cũng tương đương với nhóm tuổi lớn hơn.
Giám đốc điều hành Albert Bourla của Pfizer cho biết: “Kể từ tháng 7, các ca nhiễm COVID-19 ở trẻ em đã tăng khoảng 240% ở Mỹ, nhấn mạnh nhu cầu tiêm chủng của sức khỏe cộng đồng.
Những kết quả thử nghiệm này cung cấp một nền tảng vững chắc để chúng tôi xin cấp phép cho vaccine dành cho trẻ em từ 5 đến 11 tuổi; và chúng tôi dự định sẽ đệ trình chúng lên FDA và các cơ quan quản lý khác một cách khẩn cấp".
Các quan chức y tế hàng đầu của Mỹ tin rằng các nhà quản lý có thể đưa ra quyết định liệu việc tiêm thuốc có an toàn và hiệu quả ở trẻ nhỏ hay không trong vòng ba tuần kể từ khi các công ty gửi yêu cầu cấp phép, hai nguồn tin nói với Reuters vào đầu tháng này.
Việc cấp phép nhanh chóng có thể giúp giảm thiểu sự gia tăng các ca nhiễm COVID-19 ở trẻ em trước biến thể Delta.
 |
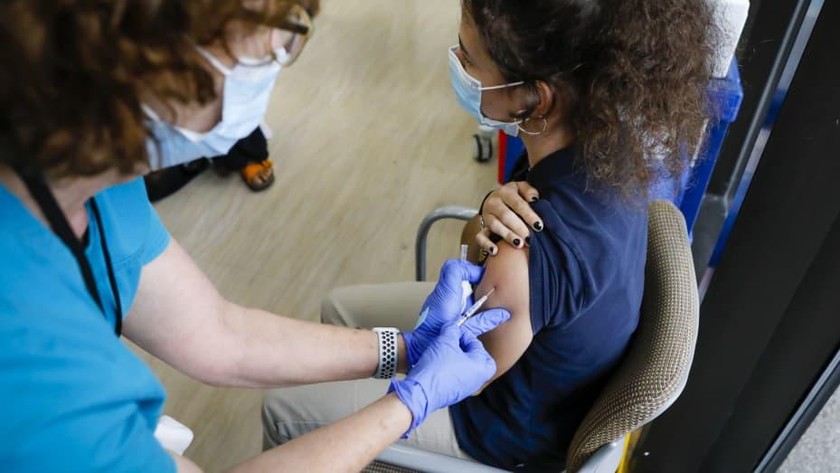
Pfizer và BioNTech sẽ nghiên cứu hiệu quả của vaccine cho trẻ từ 6 tháng tuổi. Ảnh: Reuters |
Vaccine của hai Công ty có tên là Comirnaty, đã được phép sử dụng cho trẻ em từ 12 tuổi ở nhiều quốc gia, bao gồm cả Hoa Kỳ. Vaccine ban đầu được phép sử dụng khẩn cấp ở những người từ 16 tuổi trở lên ở Hoa Kỳ vào tháng 12/2020 và đã nhận được sự chấp thuận đầy đủ của Hoa Kỳ trong nhóm tuổi đó vào tháng trước.
Hơn 2.200 trẻ em từ 5 đến 11 tuổi tham gia thử nghiệm đã được tiêm hai mũi vaccine với liều lượng 10 microgram, bằng một phần ba liều lượng đã được tiêm cho những người từ 12 tuổi trở lên. Người phát ngôn của Pfizer cho biết do chưa có đủ trường hợp nhiễm COVID-19 trong số những người tham gia nên chưa thể khẳng định hiệu quả của vaccine.
Các công ty dự kiến sẽ có dữ liệu về hiệu quả hoạt động của vaccine ở trẻ em từ hai đến năm tuổi và trẻ em từ sáu tháng đến hai tuổi sớm nhất vào quý IV năm nay.
Người phát ngôn của Pfizer cho biết vaccine này có hiệu quả khoảng 95% trong thử nghiệm lâm sàng dành cho người lớn, nhưng khả năng miễn dịch suy giảm sau vài tháng kể từ liều thứ hai. Do đó, các cơ quan quản lý của Hoa Kỳ dự kiến sẽ cho phép tiêm liều nhắc lại thứ ba của loại vaccine này cho những người lớn tuổi và có nguy cơ cao vào đầu tuần này.