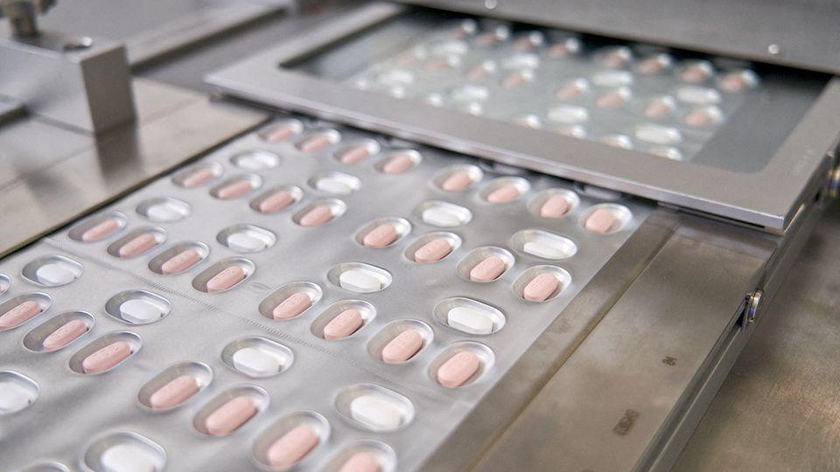
Đây là phương pháp điều trị bằng thuốc (qua đường uống) tại nhà đầu tiên, cũng như thêm một "vũ khí" mới chống lại biến thể Omicron lây lan nhanh.
Theo dữ liệu từ thử nghiệm lâm sàng của công ty, phác đồ kháng virus của Pfizer, Paxlovid, có hiệu quả gần 90% trong việc ngăn ngừa nhập viện và tử vong ở những bệnh nhân có nguy cơ mắc bệnh nặng. Dữ liệu phòng thí nghiệm gần đây cho thấy thuốc vẫn giữ được hiệu quả chống lại Omicron, Pfizer cho biết.
Pfizer đã nâng dự kiến sản xuất năm 2022 lên 120 triệu liệu trình điều trị từ 80 triệu và cho biết họ đã sẵn sàng bắt đầu giao hàng ngay tại Hoa Kỳ. Chế độ điều trị gồm hai loại thuốc bao gồm một loại thuốc mới và một loại thuốc kháng virus cũ hơn được gọi là ritonavir.
Chính phủ Hoa Kỳ sẽ có 265.000 liệu trình điều trị vào tháng Giêng và nguồn cung sẽ tăng lên trong những tháng tiếp theo, điều phối viên phản ứng COVID-19 của Nhà Trắng Jeff Zient nói trong một cuộc họp báo. Chính phủ dự kiến sẽ nhận được 10 triệu liệu trình mà họ đã đặt hàng trong vòng sáu tháng.
Amesh Adalja, học giả cấp cao tại Viện An ninh Y tế Johns Hopkins cho biết: “Sự chấp thuận thuốc Paxlovid là một cột mốc quan trọng đánh dấu một bước nữa trong việc biến COVID-19 trở thành một bệnh lây nhiễm dễ kiểm soát hơn nhiều". Tuy nhiên, bà Adalja dự báo hai vấn đề chính vẫn còn tồn tại: thuốc sẽ khan hiếm trong những tuần tới và việc sử dụng tối ưu nó đòi hỏi chẩn đoán nhanh chóng.
Pfizer cho biết họ có 180.000 liệu trình điều trị sẵn sàng xuất xưởng trong năm nay. Hợp đồng của chính phủ Hoa Kỳ cho 10 triệu liệu trình thuốc có giá $ 530 cho mỗi liệu trình.
Quyết định của Cơ quan Quản lý Thực phẩm và Dược phẩm về việc cấp phép khẩn cấp cho việc điều trị được đưa ra khi Hoa Kỳ chống lại sự gia tăng các trường hợp COVID-19 do biến thể Omicron gây ra, với việc Tổng thống Joe Biden công bố kế hoạch mở thêm các địa điểm tiêm chủng và thử nghiệm liên bang.
William Schaffner, chuyên gia hàng đầu về bệnh truyền nhiễm từ Trường Y Đại học Vanderbilt, cho biết loại thuốc klháng virus vừa được cấp phép có thể lấp đầy khoảng trống điều trị do biến thể Omicron gây ra. Ông nói, các phương pháp điều trị kháng thể đơn dòng được sử dụng rộng rãi nhất cho COVID-19 đã được chứng minh là kém hiệu quả hơn trong việc chống lại biến thể và nguồn cung cấp cho một phương pháp điều trị còn lại có hiệu quả là rất hạn chế.
Kháng thể đơn dòng thường được tiêm tĩnh mạch trong bệnh viện, không được phổ biến rộng rãi và có giá cao hơn gấp đôi so với viên thuốc Pfizer.
 |
Một nhân viên của Pfizer kiểm tra các thùng chứa thuốc Paxlovid điều trị COVID-19, tại một cơ sở phân phối ở Memphis, Tennessee, Hoa Kỳ. Ảnh: Reuters |
FDA cho biết họ đã cho phép Paxlovid sử dụng khẩn cấp để điều trị bệnh từ nhẹ đến trung bình ở người lớn và trẻ em từ 12 tuổi trở lên, những người có nguy cơ cao tiến triển thành COVID-19 nặng.
Thuốc này chỉ được bán theo đơn và phải được bắt đầu điều trị càng sớm càng tốt sau khi chẩn đoán COVID-19 và trong vòng năm ngày kể từ khi bắt đầu có triệu chứng. Những viên thuốc được uống 12 giờ một lần trong năm ngày.
Pfizer cho biết, trong khi các thử nghiệm lâm sàng không bao gồm bệnh nhân dưới 18 tuổi, chế độ dùng thuốc dành cho người lớn được phép dự kiến sẽ dẫn đến nồng độ thuốc trong máu có thể so sánh được ở bệnh nhi từ 12 tuổi trở lên nặng ít nhất 40 kg (88,2 lbs).
Loại thuốc thứ hai, ritonavir, được biết là có tương tác với một số loại thuốc kê đơn khác. Pfizer đã nói rằng điều đó có thể kiểm soát được và đề xuất rằng hầu hết bệnh nhân có thể giảm liều các loại thuốc khác của họ trong khi được điều trị COVID-19.
Pfizer cho biết họ có kế hoạch nộp đơn đăng ký thuốc mới với FDA vào năm 2022 để tìm kiếm sự chấp thuận đầy đủ về quy định.
Pfizer đã đồng ý cho phép các nhà sản xuất chung cung cấp các phiên bản điều trị cho 95 quốc gia có thu nhập thấp và trung bình thông qua thỏa thuận cấp phép với nhóm y tế công cộng quốc tế Medicines Patent Pool (MPP).
Ngoài ra, FDA cũng đang xem xét cấp phép cho thuốc của Merck & Co (MRK.N) có tên molnupiravir, được phát triển với Ridgeback Biotherapeutics, được chứng minh giảm 30% nguy cơ nhập viện và tử vong trong một cuộc thử nghiệm.
Cổ phiếu của Pfizer đã tăng hơn 1% ở mức 59,45 đô la vào thứ Tư.